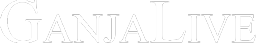:big_smiles_151:СПОСОБ ПРИМЕНЕНИЯ: Совместно с азотными и фосфорными удобрениями весной при подготовке почвы вносят под огурцы, томаты 7-10 г/м2, под другие овощные и декоративные культуры 12-15 г/м2, плодовые деревья 30-35 г/м2 приствольного круга. Корневые подкормки в течение вегетации проводят раствором сульфата магния из расчета 25 гр/10 л воды, каждые 15-20 дней. Для внекорневых подкормок (опрыскиванием) используют рабочий раствор 15 гр/10 л воды. Описание с упаковки
Отправлено с моего iPhone используя Tapatalk
Приложение
Как установить приложение на iOS
Смотрите видео ниже, чтобы узнать, как установить наш сайт в качестве веб-приложения на домашнем экране.
Примечание: В настоящее время эта функция требует доступа к сайту с помощью встроенного браузера Safari.
Приложение
Как установить приложение на iOS
Смотрите видео ниже, чтобы узнать, как установить наш сайт в качестве веб-приложения на домашнем экране.

Примечание: В настоящее время эта функция требует доступа к сайту с помощью встроенного браузера Safari.
Вы используете устаревший браузер. Этот и другие сайты могут отображаться в нём некорректно.
Вам необходимо обновить браузер или попробовать использовать другой.
Вам необходимо обновить браузер или попробовать использовать другой.
Help! Расчёт удобрений
- Автор темы Rude_Boy 69
- Дата начала
Чего угараешь? Объяснить не судьба? Я для этого за помощью и обратился. Обьясни разницу сульфата от нитрата:big_smiles_151:
Отправлено с моего iPhone используя Tapatalk
Чего угараешь? Объяснить не судьба? Я для этого за помощью и обратился. Обьясни разницу сульфата от нитрата
Отправлено с моего iPhone используя Tapatalk
Введение, основные понятия
Что есть та самая привычная нам, но мало понятная жёсткость воды? Тут я много копипастить не буду, и дам выдержки из статей по теме, а также ссылки на них для самостоятельного изучения.
Используемые далее сокращения:
- ОЖ – общая жёсткость воды; определяется присутствием в воде растворенных солей кальция и магния.
- КЖ – карбонатная жёсткость; определяется наличием в воде растворенных гидрокарбонатов.
Буферность жесткой воды
Необычайная подвижность системы, которую представляет собой вода с общей и карбонатной жесткостью, её способность постоянно менять в зависимости от условий количественный состав компонентов, как это ни парадоксально, придают ей значительную инерционность относительно рН. В химии такую инерционность называют буферностью. Под буферностью понимают способность жесткой воды менять значение рН в достаточно узком диапазоне при значительном изменении концентрации ОЖ и КЖ.
Таким образом, для создания раствора, не склонного к скачкам pH, нужна вода с довольно высокими и примерно равными значениями ОЖ и КЖ.
В воде всегда есть растворённый карбонат кальция Ca CO?3 – мел, который и даёт всем известную мутную взвесь в растворе. При закислении раствора ниже pH, равного 11, и при наличии в воде растворенного углекислого газа CO2 карбонат кальция вступает с ним в реакцию, превращаясь в доступный для растений гидрокарбонат кальция Ca(HCO3)2:
Ca CO?3 + CO2 + H2O → Ca(HCO3)2
Гидрокарбонат кальция определяют временную (гидрокарбонатную) жёсткость воды (водного раствора), поднимает карбонатную жёсткость и содержание кальция, при этом именно гидрокарбонат кальция лучше всего усваивается растениями, нуждающимися в кальции.
Основной недостаток применения сульфата магния
Что же происходит, когда мы добавляем в наш вкусный и питательный раствор такого полезного гидрокарбоната кальция Ca(HCO3)2 свой не менее полезный для генерации хлорофилла сульфат магния Mg SO?4 (доступная для растений форма Mg)?
Основной недостаток применения сульфата магния для питания растений под корень: сульфат магния вступает в реакцию с гидрокарбонатом кальция Ca(HCO3)2, в результате образуя совершенно бесполезный нерастворимый осадок гипса и доломита:
Ca(HCO3)2 + Ca CO?3 + Mg SO?4 → Ca Mg?(CO3)2↓ + Ca SO?4↓ + H2O + CO2
То есть, сульфат магния фактически блокирует доступный в воде и почве кальций, более того, блокируя и себя самого. Кроме того, добавляя соль магния в раствор, мы повышаем общую жесткость (ОЖ), что приводит к снижению pH (закислению раствора) и понижению карбонатной жёсткости (КЖ), что приводит к неустойчивости и без того упавшего pH.
Итак, поливать растение раствором сульфата магния под корень не то, что бесполезно, а даже вредно! Чаще всего даже опытные садоводы не могут определить первопричину того комплекса нарушений развития растения (некрозы, хлорозы, увядание), которые вызваны банальным поливом растения сульфатом магния под корень и последующими блокировками кальция и магния, резким понижением pH раствора (закислением почвы) и pH-дестабилизацией со скачками pH по всему доступному диапазону.
Решение проблемы
Решение проблемы очень просто для тех, кто растит на земле:
- использовать сульфат магния только для опрыскивания
или
- для внесения магния вместо сульфата магния использовать нитрат магния Mg(NO3)2; для внесения кальция – нитрат кальция Ca(NO3)2. При этом, однако, не стоит забывать о том, сколько там азота.
А вот что делать тем, кто растит на гидропонике, тема для более обстоятельной статьи: «Приготовление раствора с гидрокарбонатным буфером». Рассматривать этот вопрос я сейчас не готов, но суть процесса состоит в том, чтобы приготовить раствор с приличным содержанием в нем гидрокарбонатов кальция, что обеспечит стабильный pH и отсутствие блокировок элементов.
хорошо обьяснил бро Хрон!Основной недостаток применения сульфата магния для питания растений под корень: сульфат магния вступает в реакцию с гидрокарбонатом кальция Ca(HCO3)2, в результате образуя совершенно бесполезный нерастворимый осадок гипса и доломита:
хорошо обьяснил бро Хрон!Основной недостаток применения сульфата магния для питания растений под корень: сульфат магния вступает в реакцию с гидрокарбонатом кальция Ca(HCO3)2, в результате образуя совершенно бесполезный нерастворимый осадок гипса и доломита:
Поделиться: