Вода и водоподготовка
Вода является основной составной частью растительных организмов. Её содержание доходит до 95% массы организма, и она участвует прямо или косвенно во всех жизненных проявлениях. Вода — это та среда, в которой протекают все процессы обмена веществ. Она составляет основную часть цитоплазмы, поддерживает её структуру, устойчивость входящих в состав цитоплазмы коллоидов, обеспечивает определённую конформацию молекул белка. Высокое содержание воды придаёт содержимому клетки (цитоплазме) подвижный характер.
Вода в биологических объектах выполняет следующие основные функции: 1.Водная среда объединяет все части организма в единое целое, начиная от молекул в клетках и кончая тканями и органами. В теле растения водная фаза представляет собой непрерывную среду на всём протяжении от влаги, извлекаемой корнями из почвы, до поверхности раздела жидкость — газ в листьях, где она испаряется. 2. Вода — важнейший растворитель и важнейшая среда для биохимических реакций. 3. Вода участвует в упорядочении структур в клетках. Она входит в состав молекул белков, определяя их конформацию. 4. Вода — метаболит и непосредственный компонент биохимических процессов. Так, при фотосинтезе вода является донором электронов. При дыхании вода принимает участие в окислительных процессах. Вода необходима для гидролиза и для многих синтетических процессов. 5. Возможно, существенную роль в жизненных явлениях, особенно в мембранных процессах, играет относительно высокая протонная и электронная проводимость структурированной воды. 6. Вода — главный компонент в транспортной системе высших растений. 7. Вода — терморегулирующий фактор. Она защищает ткани от резких колебаний температуры благодаря высокой теплоёмкости и большой удельной теплоте парообразования. 8. Вода — хороший амортизатор при механических воздействиях на организм. 9. Благодаря явлениям осмоса и тургора (напряжения) вода обеспечивает упругое состояние клеток и тканей растительных организмов
Требования к воде, используемой для полива при выращивании в земле
- Идеальной для растишек является вода с нейтральной реакцией pH, не содержащая хлора и прочих вредных примесей;
- Если есть возможность, почаще проверяйте pH воды, чтобы избежать незаметного изменения pH почвы; - Лучше всего использовать воду комнатной температуры, или на 1—3° теплее комнатной, чтобы не подвергать корневую систему растений температурному стрессу;
- Так как водопроводная вода содержит хлор и другую химию, перед использованием её лучше отстаивать в течение нескольких дней в открытой ёмкости;
- Кипячёная или дистиллированная вода не повредит растениям, но в ней нет некоторых веществ, необходимых растишкам для лучшего роста;
- Дождевая вода содержит азот и другие элементы, поэтому для растений закрытого грунта такая вода, если она в экологически благополучном регионе, полезнее всего.
Химический состав воды и его влияние на качество питательного раствора в системах гидропоники.
Обладая энергоинформационной памятью, вода является регулятором всех физиологических функций растений и даже самой их жизни. Вода - это универсальный растворитель, благодаря чему все вещества, поступающие с водой в растворённом виде, не теряют свои полезные свойства и не изменяют свой химический состав. Именно основываясь на этом свойстве воды, готовят питательные растворы в гидропонике. Но, зададимся вопросом, всякая ли вода подходит для приготовления питательных растворов?
Для начала рассмотрим требования, которым должна отвечать вода, используемая при гидропонной культивации растений:
• Содержание солей и минеральных веществ в воде должно быть минимальным. Вода должна быть мягкой, свободной от солей кальция и магния. Например, высокое содержание солей кальция в воде приводит к тому, что важнейшие элементы питания - фосфор, железо, марганец, алюминий, бор переходят в соединения, которое растения не могут усвоить;
• Присутствие токсичных примесей, инородных включений и растительных ядов недопустимо;
• Реакция среды должна быть нейтральная или слабокислая. В таком случае какая вода подойдёт? Водопроводная, колодезная или из скважины, речная или озёрная, дождевая или дистиллированная? Естественно, что каждый вид воды обладает своими особенностями и характеристиками, которые указывают на степень её пригодности для приготовления питательного раствора.
Водопроводная вода вполне подходит для приготовления питательного раствора. Эта вода проходит фильтрацию и различные стадии очистки, что делает её пригодной даже для питья. Содержание в ней минеральных веществ невелико. Тем не менее она может содержать вредные для растений гербициды, тяжёлые металлы, различные соли, которые делают воду жёсткой. В зависимости от сезона, в ней может значительно увеличиваться содержание хлора. Перед применением водопроводной воды, её отстаивают в открытом сосуде в течение 2—3 дней. За это время хлор быстро испаряется и некоторые соли оседают.
Колодезная вода или вода из скважины отличается высоким содержанием железа, марганца, солей и минеральных веществ, которые вымываются из толщи грунта. Поэтому она является очень жёсткой. Некоторые источники воды содержат большое количество сероводорода, сульфатов и карбонатов. Заключение о наличии вредных составляющих в составе такой воды и её анализ можно получить у местных органов СЭС. Колодезную воду, так же как и водопроводную надо фильтровать, или отстаивать.
Речная или озёрная вода менее всего подходит в качестве воды для приготовления питательного раствора, так как в водоём могут попасть отходы промышленности и производства. В такой воде могут присутствовать продукты химических реакций, различные бактерии, патогенные микроорганизмы, продукты гниения и другие нежелательные примеси. Речную и озёрную воду принято хлорировать, а затем отстаивать. Иногда используют перекись водорода малой концентрации, что даже благотворно влияет на рост растений, так как после такой обработки, увеличивается содержание кислорода в воде 2H2O2 (перекись водорода) = 2H2O (вода) + O2 (кислород). Но для лучшей очистки все же необходимо приобрести более сложные системы фильтрации. Только после очистки при помощи таких систем речная вода может спокойно использоваться в гидропонном растворе. Но к сожалению, данные системы требуют больших денежных затрат, что делает нерентабельным использование воды из водоёмов в гидропонике.
Дождевая вода является оптимальным вариантом для приготовления питательного раствора. Она мягче всех вышеперечисленных типов воды, в ней высокое содержание кислорода, а реакция среды практически нейтральна. Но нельзя забывать о загрязнённости окружающей среды в целом из-за чего дождевая вода может содержать вредные химические соединения, тяжёлые металлы, известковую пыль (которая повышает жёсткость воды), продукты сгорания жидкого и твёрдого топлива в виде сажи и капелек маслянистой жидкости – все это сильно снижает полезные качества дождевой воды. При сборе дождевой воды следует соблюдать ряд правил. Вода, стекая по крыше, желобам и водосточным трубам, попадает в резервуар. Лучше собирать воду с крыш, выполненных из инертных материалов (глиняная черепица, шифер, или цемент, не содержащих искусственных красителей), чтобы избежать попадания вредных веществ и частиц. Не рекомендуется собирать воду с крыш, покрытие которых может содержать свинец или асбест. Непригодными являются сливы и желоба, содержащие свинец или медь. Лучшие варианты сливов - трубы из ПВХ или оцинкованной стали. Что касается резервуаров по сбору дождевой воды, лучше использовать ёмкости, сделанные из материалов устойчивых к окислению, к действию кислот, щелочей и т. д. (бетон, полиэтилен, оцинкованная сталь, стекловолокно). После длительных засушливых периодов, не используйте воду, выпавшую в первые полчаса, так как примерно за это время смывается вся накопившаяся на крыше и желобах грязь. Собрав дождевую воду, все же необходимо провести её анализ, и только после этого определить её пригодность для приготовления питательного раствора.
Дистиллированная вода практически полностью очищена от растворенных в ней минеральных солей, органических и других примесей. В этой воде нет бактерий и патогенных микроорганизмов. В ней также отсутствуют и микроэлементы. Производят её методом выпаривания пресной воды с последующей конденсацией пара в специальных устройствах, называемых дистилляторами. В результате чего все инородные вещества остаются в осадке. Одним словом, такая вода идеальна для приготовления питательных растворов. Но процесс дистилляции медленный, а аппараты рассчитаны на небольшие объёмы воды, при этом потребляя большое количество электроэнергии. Для гидропоники промышленных масштабов, где требуются сотни литров воды, это не лучший вариант.
Осмотическая вода. Что такое осмос? Выпивая при муках жажды стакан обычной воды, мы производим это соприкосновение двух растворов: воды и наших живых клеток. Оболочки клеток осуществляют функции мембран, обладающих пропускающей способностью для воды и задерживающих, содержащиеся в ней вещества. Вода в качестве менее концентрированного раствора переходит в клетки, так как живые клетки в более плотный раствор, до полного уравновешивания плотностей обоих растворов.
Осмос дал повод для размышления над использованием его и вне организма, учитывая конечный результат: живые клетки получают отфильтрованную воду природным способом. В конце прошлого века такой способ был изобретен и получил название обратного осмоса. Обратный осмос происходит в противоположном направлении: растворитель с большей плотностью через полупроницаемую мембрану переходит на молекулярном уровне в растворитель с меньшей концентрацией. Необходимо только создать давление, превышающее осмотическое. То есть происходит процесс, обратный обычному осмосу. С учетом этих особенностей и были разработаны мембраны обратного осмоса. При обратном осмосе вредные вещества скапливаются на одной стороне мембраны, а чистая вода собирается по другую сторону. Традиционные методы фильтрации не дают такой высокий результат очистки воды.
Полученное устройство, основанное на принципе обратного осмоса, называют системой обратного осмоса. Системы осмос для фильтрации воды нашли широкое применение не только в быту, но и в ряде производств. Очистка воды происходит на заложенном природой механизме, учтенном при разработке систем осмос человеком. Степень чистоты воды и освобождения ее от примесей составляет 99,9% плюс отсутствие накипи при использовании в нагревательных приборах.
Обратноосмотическая вода более предпочтительная для приготовления растворов в гидропонике, потому что имеет низкий, практически нулевой ppm. Это, в свою очередь. позволяет внести больше элементов в раствор, не боясь превысить рекомендованные для различных стадий развития растения ppm.
Подводя черту под вышесказанным, можно сказать, что какой бы тип воды вы ни выбрали, необходимо её проанализировать на содержание химических элементов. Это можно сделать самостоятельно или же отдать пробы воды в специализированное учреждение. Второй вариант более точен, хотя и требует некоторых финансовых затрат. Не всегда удаётся самостоятельно определить точный состав воды. Это можно сделать, либо измерив электропроводность нашей пробы воды, либо же купив тесты (химические реактивы) для определения содержания в анализируемой воде каждого из 13 элементов, необходимых для развития растений. Используя тесты, можно получить хорошие результаты. Но химические реактивы достаточны дорогие и их обычно хватает на небольшое количество замеров. Из измерения электропроводности, мы определяем только общее содержание элементов и не получаем никакой информации о содержании каждого элемента в отдельности в анализируемой пробе воды. После получения результаты анализа пробы воды, и определения её рН, нужно приготовить питательный раствор с учётом содержания в воде химических элементов.
Качество воды и её основные характеристики
Химически чистая вода с формулой Н₂О — это идеал, никогда не достижимый в природных условиях. Главное, природное качество воды — универсальный растворитель, поэтому в ней постоянно присутствуют в растворённом виде различные соединения, элементы, ионы и газы. Количественный и качественный состав природной воды зависит от географических условий местности и строения водоносных горизонтов.
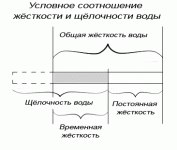
Жёсткость — комплексный показатель, в большей степени зависящий от концентрации в воде ионов кальция и магния. Количественно измеряется в мг-экв/л (миллиграмм-эквивалент на литр). Вода глубоких подземных источников имеет более высокую жёсткость (8— 10 мг-экв/л), а поверхностных источников — относительно небольшую (3— 6 мг-экв/л).
Минерализация – это суммарный количественный показатель содержания растворённых в воде веществ. Этот параметр также называют содержанием растворимых твёрдых веществ или общим солесодержанием, так как растворённые в воде вещества находятся именно в виде солей. В Европе минерализацию ещё называют как общее количество растворённых частиц – Total Dissolved Solids (TDS), что по сути, то же самое. За единицу уровня минерализации принято считать миллиграмм на литр (мг/л). Это означает вес всех растворённых веществ (в миллиграммах) в 1 литре воды. Также уровень минерализации может выражаться в частицах на миллион частиц воды – сокращённо ppm (parts per million – частиц на миллион). Такую аббревиатуру можно встретить в европейских источниках. Это означает количество частиц, растворённых в 1 миллионе частиц воды. Соотношение между единицами измерения мг/л и ppm практически равное – 1 мг/л = 1 ppm.
Существуют различные способы измерения концентрации раствора. Проще всего приобрести цифровой TDS-метр. При помощи этого прибора можно узнать ppm раствора в считаные секунды. Следует только снять колпачок, включить прибор и опустить на несколько секунд в раствор, слегка помешивая раствор прибором. Секунд через 5, когда показания установятся, можно записывать значения. Измерения также часто проводят при помощи кондуктометра, который измеряет EC (от англ. Electrical Conductivity). EC измеряется в таких единицах, как Сименсы. На самом деле и тот и другой приборы измеряют электрическую проводимость, но TDS-метр переводит измеренные значения в ppm при помощи встроенной в прибор таблицы.
рН - Возможно, один из наиболее невыявленных аспектов садоводства. рН очень важен как в гидропонном, так и в органическом, и обычном “земляном” садоводстве.
pH лучше всего измерять электронным рН тестом, однако, его нужно периодически калибровать, т. е. помогать прибору установить соотношение между сигналом от электрода и значением рН с помощью калибровочного раствора. Также большой популярность пользуется простой и доступный рН тестор от GHE, который определяет кислотно-щелочной баланс при помощи реагента.
рН измеряется в шкале от 1 до 14, значение рН7 считается нейтральным. Кислоты имеют значения ниже 7, а щёлочь (основания) выше.
Технически, термин рН относится к potential водороду – гидроксильному иону, содержащемуся в растворе. Растворы ионизируются в положительные и отрицательные ионы. Если раствор имеет больше водородных (положительных) ионов, чем гидроксильных (отрицательных) ионов, тогда это кислота (1–6.9 по шкале рН). И наоборот, если раствор имеет больше гидроксильных ионов, чем ионов водорода, раствор – щёлочь (или основание), с диапазоном 7.1–14 по шкале рН. Чистая вода имеет баланс водородных (H+) и гидроксильных (О-) ионов и – поэтому имеет нейтральный рН (рН 7). Когда вода менее чистая, она может иметь рН или выше или ниже 7. Шкала pH логарифмическая, что означает, что каждая единица изменения равняется десятикратному изменению концентрации ионов водорода/гидроксила. Другими словами, раствор с pH 6 в десять раз более кислый, чем раствор с pH 7, и раствор с pH 5 будет в десять раз более кислый, чем раствор с pH 6 и в сто раз более кислый, чем раствор с pH 7. Это означает, что когда вы регулируете pH вашего питательного раствора, и вам необходимо изменить pH на два пункта (например с 7.5 до 5.5) вы должны использовать в десять раз больше исправителя pH, чем если бы изменяли pH только на один пункт (с 7.5 до 6.5).
Почему важен pH? Когда pH не на надлежащем уровне, растение начнёт терять способность поглощать некоторые из обязательных элементов, необходимых для здорового роста. Для всех растений есть специфический уровень pH, который производит оптимальные результаты.
Подготовка воды для использования в системах гидропоники
Как известно при посадке растений в грунт, особенно на рассаду, землю обеззараживают различными средствами. Это позволяет избавиться от личинок вредителей, грибка и различных бактерий. Аналогичный процесс необходимо провести и для воды, используемой в гидропонной установке. Впрочем, помимо обеззараживания необходимо предусмотреть ещё и систему фильтрации, которая позволит механически удалить нежелательные примеси в воде. При этом используется сразу два фильтра — один для предварительной механической очистки, который устанавливают в системе перед ультрафиолетовым стерилизатором, а второй фильтр тонкой очистки, что позволит удалить все погибшие во время обеззараживания микроорганизмы. Применять подобную систему можно не только в гидропонных установках. При необходимости они могут быть использованы для подготовки воды для систем капельного полива в теплицах при выращивании брокколи или других овощей, где качество воды также имеет большое значение.
Методы фильтрации и типы фильтров
Первым этапом по удалению примесей является процесс механической очистки. Для него устанавливают фильтр грубой очистки воды. А для большей эффективности следом монтируют фильтр тонкой очистки воды. Воду из колодцев и скважин тоже нельзя назвать идеально чистой. Не верите? Отнесите её на экспертизу и убедитесь. Вода из скважины может содержать растворенное железо, магний, кальций. В колодцах ко всему прочему есть вероятность загрязнения воды нитратами и микроорганизмами.
Фильтры механической очистки воды. Устанавливают фильтры механической очистки воды в начале всех технических устройств. Они выполняют функцию первичного удаления из жидкости нерастворимых частиц. Выбирать модель устройства необходимо, исходя из конкретных требований. Перед покупкой определяются с условиями эксплуатации и сферой применения. Это поможет выяснить технические характеристики необходимого оборудования.
Фильтры грубой очистки воды. Фильтр грубой очистки удаляет из воды нерастворимые фракции, такие как глина, песок, ржавчина и подобные вещества. Оттого какое содержание примесей имеется в воде, зависит выбор того или иного типа фильтра. Принцип действия у всех устройств этого вида схож. Грубые частицы задерживаются в самом фильтре, а очищенная от них вода поступает в трубопровод. По мере заполнения устройство снимается, вычищается и устанавливается на место. Работа фильтра не предусматривает применения химических реагентов, она основана на механическом действии. Выбор фильтра зависит от производительности системы (объём потребляемой жидкости в час) и массы твёрдых фракций. Различают три вида фильтров грубой очистки воды:
сетчатый
картриджный
высокоскоростной напорный.
Сетчатый фильтр
Рабочий элемент такого фильтра — мелкозернистая сетка. Основа конструкции сетчатого фильтра – сетка с ячейками 50-500 мкм. Сетчатые фильтры бывают непромывные и самопромывные. Первые периодически по мере загрязнения снимают и вычищают. Для этого необходимо отключать систему водоснабжения и разбирать сам фильтр. Вторые не надо разбирать и очищать. Они потому и называются самопромывными, что избавляются от нерастворимых частиц в автоматическом режиме. Для них устанавливают дренажную трубу, в которую сливается грязная вода после самоочищения устройства. Фильтры, устанавливаемые на холодную воду, делаются из прозрачного материала. Для горячего водоснабжения выпускаются приборы с металлическим корпусом способным выдерживать высокую температуру. К некоторым видам сетчатых фильтров, на выходе, устанавливают клапан контроля давления и манометр. Клапан защищает бытовые приборы от гидравлических ударов и скачков давления воды. Манометр показывает давление в трубопроводе.
Картриджный фильтр
Главным элементом картриджного фильтра является сменный картридж или патрон, помещённый в колбу из стали или пластика. Такое устройство задерживает примеси размером от 0,5 мкм. Корпус изделия для холодной воды изготавливается из прозрачного материала. Это позволяет определять необходимость замены патрона. Фильтры для горячей воды имеют непрозрачный корпус. Картриджи могут быть выполнены из различных материалов. Патроны из специального волокна задерживают хлор, а картриджи чулочного типа не пропускают примеси имеющие волокнистую структуру (вязкая глина, тина, водоросли).
Высокоскоростной напорный фильтр
Такой фильтр позволяет отрегулировать размер задерживаемой фракции. Если в источнике воды находится много примесей разнородной структуры, универсальным устройством для очистки послужит высокоскоростной напорный фильтр. Состоит такое изделие из ёмкости, выполненной из антикоррозийного материала, которая заполняется фильтрующим материалом. Проходя через прибор, вода очищается от нерастворимых фракций размером от 30 мкм. Вверху ёмкости установлен автоматический регулирующий блок. Он отвечает за процесс фильтрации и сохранение свойств материала. Дополнительно к фильтру подсоединяют дренажный трубопровод. Установка высокоскоростного напорного фильтра связана с небольшими неудобствами. Он имеет большие габариты. Размещать его можно только в теплом помещении.
Фильтры тонкой очистки
После грубой очистки воды в ней все ещё остаются мелкие примеси. Это могут быть взвеси тяжёлых металлов, соединения химических элементов и даже небольшие микроорганизмы. Избавить воду от этих примесей помогут фильтры тонкой очистки. Фильтры тонкой очистки воды способны задерживать микрочастицы размером от 5 мкм. Обычно их устанавливают после фильтров грубой очистки. Такая двухступенчатая система даёт качественный продукт на выходе. В качестве рабочего элемента таких устройств могут выступать:
сорбционный материал;
обратноосмотическая мембрана
ионообменные смолы.
Сорбиционный фильтр
Сорбционный фильтр позволяет очистить воду от тяжёлых металлов. Сорбционный фильтр используется для очищения воды от тяжёлых металлов (даже железа и свинца), хлорорганических соединений, микроорганизмов. Он способен избавить воду от неприятных запахов. Состоит сорбционный фильтр из резервуара, изготовленного из пластика и наполненного сорбентом. В качестве сорбента могут выступать алюмосиликат или активированный уголь. Фильтр имеет небольшой размер, довольно прост в установке, легко демонтируется при замене картриджа. Недостатком этого устройства является низкая скорость фильтрации и необходимость частой замены картриджа.
Обратноосмотический фильтр
Обратноосмотический фильтр состоит из нескольких последовательно соединённых стальных или пластиковых резервуаров. Активным компонентом таких фильтров является мембрана, изготовленная из полимерного материала. Она очень чувствительна к составу воды и разрушается под действием хлора. Поэтому для обратноосмотических фильтров необходима система предочистки, в качестве которой применяется ультрафильтрационный модуль или фильтр грубой очистки. Обратноосмотический фильтр часто снабжают ультрафиолетовым блоком для дополнительного обеззараживания. Недостатком такой системы очистки является необходимость минимального давления воды в 3,5 атмосфер. Если давление ниже, необходимо устанавливать насос. Из-за малой производительности обратноосмотический фильтр снабжается накопительным баком для хранения очищенной воды. Все это окупается высокой степенью очистки.
Ионообменный фильтр
Ионообменные фильтры применяют для смягчения воды и удаления из неё органических соединений. Корпус такого изделия изготавливается из пластика или стали. Внутрь помещён фильтрующий резервуар, наполненный ионообменной смолой. Производительность устройства зависит от объёма фильтрующей загрузки. Ионообменный фильтр тонкой очистки позволяет смягчить воду путём изменения её pH. Недостатком таких изделий является дополнительное использование регенерирующих баков, постоянное применение солевых растворов и утилизация использованных компонентов. Эффективность ионообменных фильтров зависит от состава поступающей жидкости, качества ионитов и температуры помещения.